Tại hội nghị đánh giá sau 2 năm thực hiện, triển khai Nghị định 36/2016/NĐ-CP về quản lý trang thiết bị y tế (TTBYT) và lấy ý kiến sửa đổi nghị định này, ông Nguyễn Minh Tuấn, Vụ trưởng Vụ Trang thiết bị và Công trình y tế - Bộ Y tế, cho biết cơ quan này đang đề xuất bãi bỏ, sửa đổi nhiều điều kiện liên quan tới việc sản xuất - kinh doanh TTBYT.
Tạo thuận lợi cho doanh nghiệp
Cũng theo ông Tuấn, sau 2 năm thực hiện Nghị định 36 và ứng dụng dịch vụ công trực tuyến trong thực hiện các nhóm thủ tục cấp phép nhập khẩu..., trên cả nước đã tiếp nhận, giải quyết và trả kết quả 10.462 hồ sơ. Cùng với đó, thời gian giải quyết đối với các thủ tục hành chính được thực hiện nhanh chóng, thuận lợi cho công tác xử lý, theo dõi và quản lý thông tin hồ sơ, các doanh nghiệp (DN) do toàn bộ công việc được xử lý trên phần mềm hệ thống trực tuyến và theo mức độ 4 về công nghệ thông tin.
Theo ông Nguyễn Tử Hiếu, phụ trách bộ phận đăng ký TTBYT Vụ Trang thiết bị và Công trình y tế, thực hiện việc cải cách thủ tục hành chính, tạo thuận lợi cho DN theo Nghị quyết 19 của Chính phủ, vụ đã triển khai 6 nhóm thủ tục công bố, đăng ký, đề nghị cấp phép trực tuyến tại Bộ Y tế (giai đoạn 1 từ ngày 1-1-2017: công bố đủ điều kiện phân loại thiết bị y tế và giai đoạn 2 từ ngày 1-7-2017 với 5 nhóm thủ tục theo Nghị định 36/2016/NĐ-CP. Tuy nhiên, một số nội dung về quản lý TTBYT chưa cụ thể, chưa rõ ràng gây khó khăn cho thanh tra, kiểm tra và cho DN.

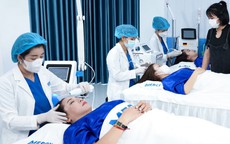
Bộ Y tế đang đề xuất cắt giảm hàng chục điều kiện kinh doanh trong lĩnh vực thiết bị y tế
Dự thảo Nghị định bổ sung, sửa đổi Nghị định 36 sẽ cắt giảm, bãi bỏ 11 điều kiện sản xuất - kinh doanh và sửa đổi 24 điều kiện sản xuất - kinh doanh TTBYT nhằm tạo điều kiện tối đa cho DN. Hiện Bộ Y tế đang phối hợp với Tổng cục Hải quan, Bộ Tài chính xây dựng dự thảo Thông tư ban hành danh mục TTBYT kèm mã số hồ sơ theo danh mục hàng hóa xuất - nhập khẩu, thuộc diện quản lý chuyên ngành của Bộ Y tế. Cũng tại dự thảo này, lần đầu tiên sẽ có các quy định nhằm quản lý chặt chẽ việc mua bán, nhập khẩu TTBYT có chứa chất gây nghiện, chất hướng thần và tiền chất. Các công ty kinh doanh mặt hàng này sẽ phải thực hiện chế độ báo cáo về xuất, nhập, tồn kho, có địa chỉ đơn vị sử dụng rõ ràng…
Tăng cường hậu kiểm
Ông Tuấn cho biết khi đã thoáng về thủ tục cho DN, việc hậu kiểm sẽ được trung tâm kiểm chuẩn giám sát thực hiện. Với những sai phạm hoặc gian lận trong lĩnh vực TTBYT sẽ bị xử phạt rất nặng.
Trong khi đó, ông Nguyễn Anh Quang, Trưởng Phòng Tài chính Sở Y tế TP Hà Nội, cho biết vừa qua, các đợt thanh tra, hậu kiểm việc sản xuất - kinh doanh sử dụng TTBYT trên địa bàn Hà Nội, cơ quan chức năng đã phát hiện nhiều vi phạm, 55 tổ chức, DN bị thu hồi công bố đủ điều kiện, 26 DN không đạt khi kiểm tra thực tế về điều kiện bảo quản TTBYT, PCCC của kho; không đạt về điều kiện vận chuyển, thậm chí đã phát hiện một số TTBYT không đủ giấy tờ về nguồn gốc xuất xứ. Tới đây, cơ quan quản lý sẽ tăng cường thanh tra hậu kiểm về chấp hành các quy định kinh doanh TTBYT, chất lượng, nguồn gốc TTBYT; có các giải pháp để kiểm soát giá TTBYT, vật tư y tế khi tham gia đấu thầu vào bệnh viện công, tránh tình trạng đẩy giá cao bất hợp lý. Hiện Sở Y tế TP Hà Nội đang đẩy mạnh ứng dụng công nghệ thông tin vào công tác quản lý, tuy nhiên, việc triển khai vẫn còn nhiều khó khăn, như chưa có quy định kiểm chuẩn định kỳ TTBYT đang sử dụng tại các cơ sở y tế; chưa có cơ quan chuyên môn về kiểm định chuẩn chất lượng TTBYT.
Tại hội nghị, các chuyên gia cũng cho biết thời gian qua cũng có những DN lợi dụng nhằm qua mặt các cơ quan chức năng để kinh doanh TTBYT chưa bảo đảm chất lượng. Đơn cử, các hình thức tạm xuất tái nhập, phá niêm phong, đánh tráo hàng ngay trên đường vận chuyển, thẩm lậu vào nội địa để tiêu thụ hoặc hàng vận chuyển đến Campuchia rồi tìm cách quay ngược về Việt Nam... là những thủ đoạn gian lận thương mại mới trong lĩnh vực TTBYT, đòi hỏi sự vào cuộc ráo riết hơn của cơ quan hải quan nhằm ngăn chặn những nguy cơ này.






Viết bình luận