
Nhiều DN dược nước ngoài bị kiểm tra 100% mẫu thuốc trước khi lưu hành
Dựa trên kết quả kiểm tra chất lượng các loại thuốc nhập khẩu theo quy định, Cục Quản lý dược, Bộ Y tế vừa có công văn gửi sở Y tế các tỉnh, thành phố và các công ty xuất nhập khẩu thuốc công bố đợt 26 danh sách 50 công ty nước ngoài có thuốc vi phạm chất lượng phải thực hiện lấy mẫu kiểm tra chất lượng đối với 100% lô thuốc nhập khẩu.
Các công ty dược này thuộc 7 quốc gia có thuốc vi phạm chất lượng phải thực hiện lấy mẫu kiểm tra. Trong đó, đứng đầu bảng vẫn là các công ty dược của Ấn Độ với 39 doanh nghiệp, tiếp đến là Pakistan, Trung Quốc, Hàn Quốc, Nga, Mỹ và Bangladesh.
Trong đợt công bố lần thứ 26 này, hầu hết là các công ty dược có vi phạm về chất lượng thuốc từ các đợt kiểm tra trước đó nên phải thực hiện lấy mẫu kiểm tra chất lượng đối với 100% lô thuốc nhập khẩu thay vì hậu kiểm như quy định.
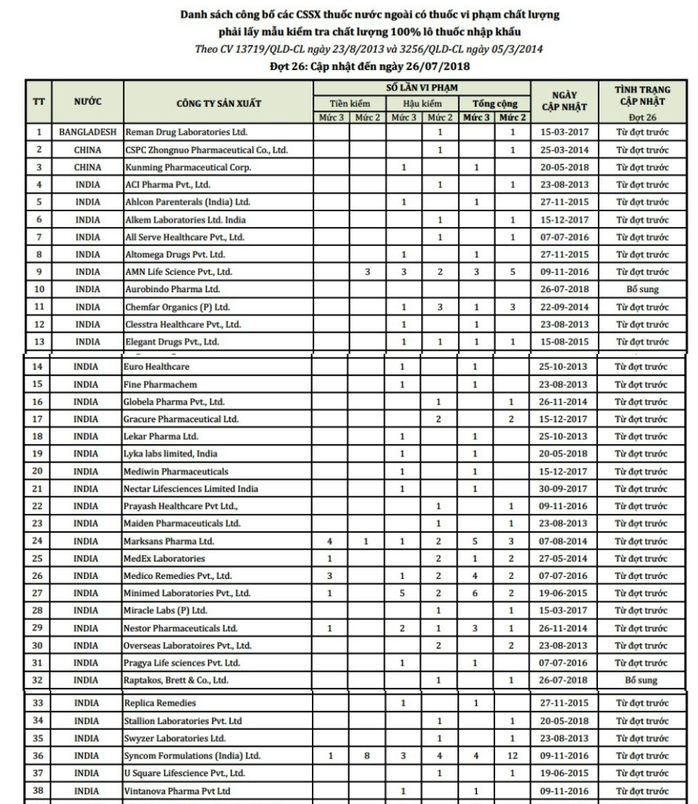
Danh sách các DN dược có thuốc phải kiểm tra 100% chất lượng
Cục Quản lý dược yêu cầu các sở Y tế tỉnh, thành phố trực thuộc Trung ương giao nhiệm vụ chỉ đạo các đơn vị thanh tra, quản lý dược và kiểm nghiệm thuốc thuộc sở tiến hành việc kiểm tra, giám sát việc chấp hành các quy định về kiểm tra chất lượng thuốc nhập khẩu lưu hành trên địa bàn quản lý và xử lý các tổ chức, cá nhân vi phạm.
Theo Cục Quản lý dược, thuốc trước khi đưa ra lưu hành trên thị trường phải được Bộ Y tế thẩm định hồ sơ đăng ký bao gồm nguyên liệu, quy trình sản xuất, tiêu chuẩn chất lượng, độ ổn định và dữ liệu lâm sàng. Nhà sản xuất phải đáp ứng điều kiện sản xuất (GMP), phải tuân thủ đúng hồ sơ đăng ký thuốc đã được phê duyệt trong quá trình sản xuất và phải kiểm tra chất lượng đáp ứng tiêu chuẩn đã được đăng ký trước khi đưa thuốc ra thị trường.
Khi đưa thuốc lưu hành trên thị trường, cơ sở sản xuất/ nhập khẩu tự giám sát và chịu trách nhiệm đối với chất lượng thuốc do cơ sở mình sản xuất, báo cáo cơ quan quản lý khi phát hiện các dấu hiệu có nguy cơ ảnh hưởng đến sức khoẻ người sử dụng và chịu sự lấy mẫu, giám sát của cơ quan quản lý.
Hằng năm, các hệ thống kiểm nghiệm lấy khoảng 40.000 mẫu thuốc trên thị trường để giám sát chất lượng (năm 2015 đã lấy 38.627 mẫu, năm 2016 đã lấy 37.219, năm 2017 đã lấy 36.362). Tỉ lệ thuốc kém chất lượng các năm gần đây khoảng 1,5 – 2,0% và tỉ lệ thuốc giả dưới 0,05%.
Cục Quản lý dược cho biết thời gian qua cơ quan này đã thực hiện kiểm tra chất lượng 100% các lô thuốc nhập khẩu của các công ty sản xuất thuốc nước ngoài đã có thuốc vi phạm chất lượng trong quá trình lưu hành thuốc tại Việt Nam.





Bình luận (0)