Ông Nguyễn Tất Đạt, Phó Cục trưởng Cục Quản lý dược - Bộ Y tế, vừa ký công văn yêu cầu thu hồi toàn bộ thuốc sản xuất từ nguyên liệu Valsartan do Công ty Zhejiang Huahai Pharmaceutical của Trung Quốc sản xuất. Trước đó, Cơ quan Quản lý dược phẩm châu Âu (EMA), Cơ quan Quản lý dược Canada và một nước thông báo về việc thu hồi số thuốc chứa Valsartan của công ty này do có tạp chất N-nitrosodimethylamine (NDMA) - nguy cơ gây ung thư.
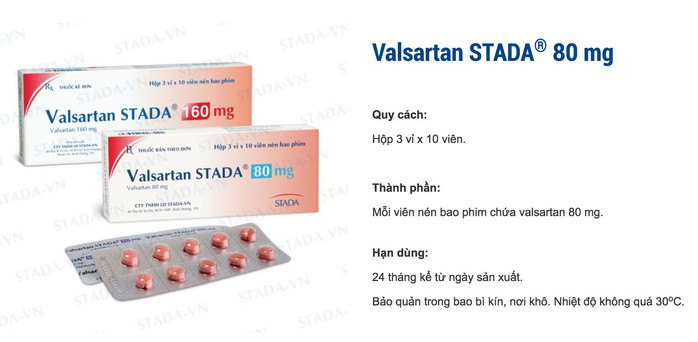
Thuốc điều trị tăng huyết áp Valsartan STADA 80 mg là một trong số 23 thuốc buộc phải thu hồi
Đến nay, thuốc sản xuất từ nguyên liệu Valsartan của Trung Quốc đã bị thu hồi tại 22 quốc gia châu Âu. Đáng chú ý, tại Việt Nam, nguyên liệu Valsartan có trong nhiều loại thuốc đang được các doanh nghiệp sản xuất và phân phối. Thuốc dùng để điều trị cao huyết áp, suy tim nhằm giảm tỉ lệ tử vong do tim mạch trên bệnh nhân suy chức năng tâm thất trái sau nhồi máu cơ tim và điều trị suy tim. Đây là thuốc thuộc nhóm phải kê đơn.
Theo rà soát của Cục Quản lý dược, 8 doanh nghiệp dược được cấp đăng ký đối với 23 thuốc thành phẩm đang lưu hành sử dụng hoạt chất Valsartan được nhập từ Công ty Zhejiang Huahai Pharmaceutical của Trung Quốc buộc phải thu hồi. Cụ thể, Công ty CP Dược phẩm Cửu Long (tỉnh Vĩnh Long) thu hồi thuốc Valsartan 80 mg (số đăng ký VD-27843-17); Công CP Dược phẩm Trung ương 2 (TP Hà Nội) thu hồi thuốc tim mạch Tolzartan Plus 160 mg (số đăng ký VD-27098-17); Công ty CP Hóa dược Việt Nam (TP Hà Nội) thu hồi thuốc tim mạch Ocedio 80 mg (đăng ký VD-29339-18); Công ty CP Dược phẩm OPV (tỉnh Đồng Nai) thu hồi 7 loại thuốc trị tim mạch, phù do suy tim và huyết áp, gồm: Opevalsart 40 mg (VD-20792-14), Vasaratim 80mg (VD-20802-14), Vasaratim Plus 160:25 (VD-12907-10), Vasaratim 40 mg (VD-20461-14) và Halotan hoạt chất 40/80/160 mg, Opevalsart 80, Vasaratim 160; Công ty CP Nhập khẩu Y tế DOMESCO (tỉnh Đồng Tháp) thu hồi 3 thuốc, gồm: Doraval 80 mg (VD-25424-16), Doraval plus 160/25 mg (VD-26463-17), Oraval plus 80/12,5 mg (VD-26464-17); Công ty CP PYMEPHARCO (tỉnh Phú Yên) thu hồi 4 thuốc Pyvasart hàm lượng 40/80/160 mg và thuốc Pyvasart HCT 80/12.5 mg; Công ty TNHH Liên doanh STADA Việt Nam (TP HCM) thu hồi 4 thuốc Valsartan STADA hàm lượng 40/80/160 mg và chi nhánh của công ty ở Bình Dương thu hồi 2 thuốc Valsartan STADA 40 mg, Valsartan STADA 80 mg.
Theo yêu cầu của Cục Quản lý dược, các công ty đăng ký thuốc, sản xuất thuốc, công ty nhập khẩu phối hợp với nhà phân phối thuốc thông báo thu hồi tất cả các lô thuốc thành phẩm trong công thức sản xuất có chứa nguyên liệu Valsartan tới các cơ sở bán buôn, bán lẻ, sử dụng thuốc. Đồng thời, ngừng ngay việc sử dụng nguyên liệu Valsartan của Công ty Zhejiang Huahai Pharmaceutical - Trung Quốc để sản xuất thuốc thành phẩm. Các doanh nghiệp gửi báo cáo việc thu hồi thuốc về cơ quan trên trước ngày 10-8.
Theo EMA, một số lượng lớn thuốc trị cao huyết áp và bệnh tim chứa hoạt chất được sản xuất tại Trung Quốc có nguy cơ gây ung thư đã bị thu hồi ở các nước châu Âu. Những nghiên cứu trên động vật cho thấy NDMA có thể gây tình trạng nhiễm độc, tạo ra các khối u và làm ảnh hưởng tới đường hô hấp. Với tỉ lệ nhất định, tạp chất này có thể gây hại cho người sử dụng, phá hủy gan và gây ung thư.




Bình luận (0)